Ya en septiembre se esperaba que este noviembre fuese un mes agitado en lo que a vacunas contra el coronavirus pandémico se refiere. Y los anuncios vienen llegando, tanto sobre resultados preliminares de ensayos clínicos avanzados como sobre las negociaciones que se llevan a cabo por parte de la Argentina con el objetivo de asegurarse dosis de las potenciales vacunas que podrían llegar a buen puerto y ser aprobadas. Las autoridades sanitarias locales negocian con cinco de los diez laboratorios que tienen candidatas vacunales en fase 3 de testeos con seres humanos.
Las negociaciones involucran tanto conversaciones como preacuerdos de compra a riesgo de millones de dosis de diferentes desarrolladores, tal y como ya vienen haciendo otros países más ricos, los Estados Unidos, Alemania, Gran Bretaña, Canadá, Japón, entre otros (amén de la Unión Europea como bloque).
En los registros de la Organización Mundial de la Salud (OMS) hay actualmente 45 vacunas en etapa de ensayos clínicos en seres humanos, 10 de ellas en la recta final, es decir en fase 3. Otras 156 (incluyendo una argentina) están en evaluación preclínica.
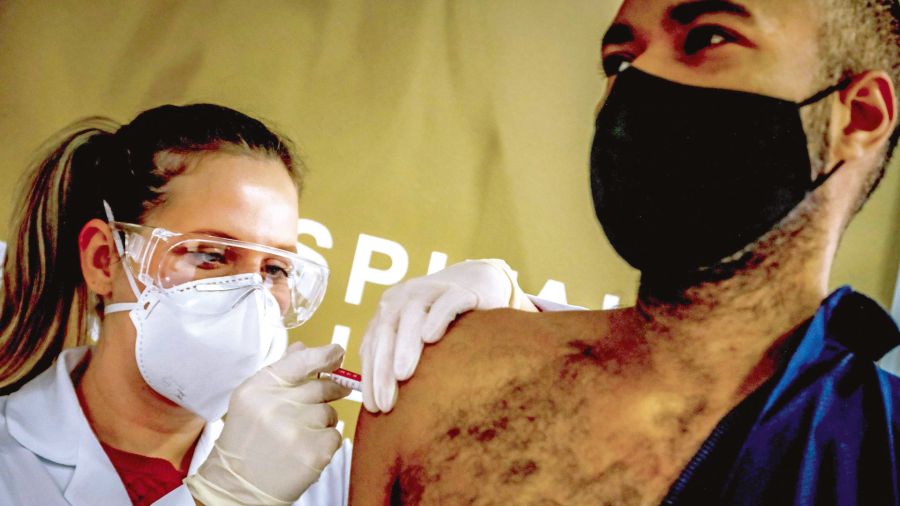
Operación vacunación masiva
En nuestro país ya comenzaron los preparativos para una eventual vacunación masiva. Durante la reunión del 29 de octubre que mantuvieron los ministros de Salud a través del Consejo Federal de Salud (COFESA) se analizaron los ítems que deberá tener en consideración cada distrito a partir de la “Planificación para la vacunación contra el nuevo coronavirus (SARS-CoV-2)”.
El documento establece que desde el lunes 9 de noviembre se comience con la presentación por parte de cada jurisdicción de un plan de acción, y las reuniones correspondientes con los “actores clave” en lo que será una megacampaña que exige contar, además de con el recurso de la o las vacunas eventualmente aprobadas, con personal calificado, materiales y equipos, infraestructura, recursos financieros, tanto para implementación de las tareas de vacunación como para el registro de las mismas y la supervisión de los resultados.
El objetivo del plan es “vacunar al 100% de la población objetivo en forma escalonada de acuerdo a la disponibilidad del recurso y la priorización de riesgo”. La primera etapa incluye al personal de salud y de seguridad (entre otros considerados estratégicos), a las personas mayores de 60 años y a aquellas de entre 18 y 59 años que tengan factores de riesgo.
Paraguas legislativo
Otra herramienta que era imprescindible para comenzar con la planificación y para el cierre de preacuerdos con laboratorios llegó también en la última semana de octubre. El Senado aprobó la Ley de Vacunas Destinadas a Generar Inmunidad Adquirida contra el COVID-19, que declara “de interés público a la investigación, desarrollo, fabricación y adquisición de las vacunas destinados a generar inmunidad” contra la enfermedad respiratoria causada por el coronavirus pandémico.
La ley, bajo el número 27.573, fue promulgada el viernes 6 de noviembre y se convierte en el marco legal que permite al Estado nacional comprar futuras vacunas, mediante contrataciones a laboratorios y a organizaciones como la alianza COVAX, una plataforma global de compra colectiva impulsada por la OMS y creada para facilitar y garantizar el acceso a una distribución equitativa de vacunas contra la Covid-19 de la cual la Argentina forma parte.
En todos los casos, las candidatas vacunales tendrán que contar con la evaluación y aprobación de organismos regulatorios competentes. Así lo establece el artículo 8 de la ley: “El adquirente de vacunas destinadas a generar inmunidad adquirida contra la COVID-19, objeto de esta ley, debe presentarlas a la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (A.N.M.A.T.) a los efectos de la intervención de su competencia y deben ser autorizadas por el Ministerio de Salud, quienes deberán expedirse en un plazo máximo treinta (30) días, previo a su uso en la población objetivo”.
El artículo 9 permite a esos organismos evaluatorios actuar en tiempos extraordinarios, tal y como ya se ha hecho en otros países: “autorízase, por la excepcionalidad del contexto pandémico, a los organismos competentes a realizar la aprobación de emergencia de las vacunas objeto de esta ley, con el debido respaldo de la evidencia científica y bioética que permita comprobar su seguridad y eficacia”.
Es decir que podrá haber conversaciones y preacuerdos, pero en la Argentina no podrá avanzarse ni en la aprobación ni en la aplicación de vacuna alguna si la misma no ha demostrado antes eficacia y seguridad en los ensayos clínicos de rigor.
La ley faculta a que haya acuerdos de confidencialidad, en el sentido de que las autoridades sanitarias argentinas conocerán toda la fórmula de una candidata vacunal, pero no pueden hacerla pública. Y es algo que los laboratorios en estos momentos están pidiendo, por razones de protección ante otros competidores.
Los contratos celebrados por el gobierno nacional con un laboratorio deberán ser remitidos a la Auditoría General de la Nación (AGN) y a las comisiones de salud de la Cámara de Diputados y del Senado.

Conversaciones
Ya en agosto de este año el Ministro de Salud de la Nación, Ginés González García, le había dicho en declaraciones a la agencia de noticias Télam que “la Argentina se encuentra negociando con distintas firmas internacionales la prioridad en la asignación de vacunas contra el coronavirus y también la transferencia de tecnología”.
El martes 3 de noviembre el ministro aclaraba en una conferencia brindada a miembros de la Red Argentina de Periodismo Científico (RadPC) que “aún no hemos confirmado ningún acuerdo, y no podremos hacerlo hasta que se promulgue la Ley. Sí tenemos negociaciones”.
Hacía referencia a los acercamientos que se mantuvieron para llegar a acuerdos en relación con la vacuna desarrollada por Pfizer/BioNTech (de la cual Argentina participa en los ensayos clínicos de fase 3), con la candidata de Oxford/AstraZeneca (para la que el país producirá entre 150 y 200 millones de dosis a ser distribuidas en América Latina exceptuando a Brasil), con la china Sinopharm (que también está llevando a cabo ensayos clínicos de fase 3 a través de la Fundación Huésped), con el laboratorio Janssen/Johnson&Johnson (que acaba de comenzar ensayos clínicos también de fase 3 en el país), y con la Federación Rusa por la vacuna Sputnik V.
La vacuna rusa
El primer preacuerdo anunciado como tal, hizo un ruido especial durante la semana pasada: compromete la adquisición de 10 millones de dosis de la vacuna SputnikV (de origen ruso, cuyo esquema exige la aplicación de dosis, con una diferencia de 21 días entre cada una) para fines de diciembre, y de otros 15 millones de dosis para enero del 2021. El costo estimado de ambas dosis sería de 19,95 dólares.
De nuevo: todo dependerá de que la vacuna avance con éxito en las pruebas clínicas que actualmente comprenden a 40.000 personas, y haya sido aprobada y registrada en los organismos competentes. El Instituto de Investigación Gamaleya, su desarrollador, solicitó una revisión de la vacuna ante la OMS.
La vacuna fue registrada en la Federación Rusa a mediados de agosto y las pruebas clínicas se llevan a acabo, además de en Rusia, en los Emiratos Árabes Unidos, India, Venezuela y Bielorrusia.
La vacuna de Oxford
Este fin de semana el laboratorio sueco británico AstraZeneca anunció la firma de un acuerdo con la Argentina para la entrega de 22 millones de dosis de la conocida como “vacuna de Oxford”. “Se espera que las entregas comiencen durante el primer semestre del 2021, en caso de que los ensayos en curso resulten exitosos y posteriores a la aprobación correspondiente por parte de las autoridades regulatorias”, señala el comunicado emitido por el laboratorio.
Esta candidata vacunal se está probando en voluntarios en el Reino Unido, los Estados Unidos, Brasil, Sudáfrica y Kenia. El ensayo fue suspendido luego de reportarse posibles efectos secundarios graves en dos particiantes de los ensayos, pero los estudios se reanudaron luego de que el laboratorio informara que esos efectos no tenían relación con la vacuna.
AstraZeneca comenzó a trabajar con la ANMAT en octubre para avanzar en un “proceso de revisión continua” para su vacuna AZD1222 (el nombre que tiene en la etapa de ensayos), una herramienta regulatoria flexible que permite avanzar en la evaluación de una vacuna o de un medicamento cuando hay una emergencia de salud pública.
En ese sentido, la Secretaria de Acceso a la Salud, Carla Vizzotti, explicó en la conferencia virtual con la RaDPC que la ANMAT está recibiendo información parcial de los resultados de los ensayos clínicos y, al mismo tiempo, trabajando con la Organización Panamericana de la Salud (OPS) para recibir datos provenientes de la OMS en relación con los resultados y la seguridad y eficacia de algunas de las vacunas. En algunos casos esa información llega en tiempo real.
"La AZD1222 fue la primera vacuna contra la Covid-19 en ser aceptada para este proceso por la Agencia Europea del Medicamento, EMA", asegura AstraZeneca, y agrega que las autoridades regulatorias de Canadá, Japón, Brasil, Suiza, Australia y Corea del Sur, "también han iniciado protocolos de revisión para la vacuna candidata”.
La candidata de Pfizer
El consorcio de los laboratorios estadounidense y alemán Pfizer/BioNTech también llegó a un preacuerdo con la Argentina, por la provisión de 3 millones de dosis en diciembre, a razón de 19 dólares. La Argentina es uno de los países en los cuales se está testeando esta vacuna, además de en los Estados Unidos, Brasil y Alemania.
En el día de hoy, Pfizer/BioNTech anunciaron tener resultados alentadores: la vacuna produce inmunidad en el 90% de quienes la reciben, 7 días después de haber recibido la segunda dosis (que se aplica a los 28 días de la primera). Esta información no ha sido publicada en revista científica ni evaluada por científicos ajenos al laboratorio, sino dada a conocer por declaraciones de los laboratorios.
El rol de Jenseen
En el caso del laboratorio Jenseen (de Johnson&Johnson), las conversaciones aún no concluyeron en un preacuerdo o acuerdo, con lo cual no hay ni cantidad de dosis (es la única que consta de una sola aplicación) ni plazos estimados. En principio, el costo sería de aproximadamente 37 dólares. Los ensayos clínicos de fase 3 se llevan a cabo desde septiembre con 60 mil voluntarios, en los Estados Unidos, Colombia, Brasil, Chile, México, Perú, Sudáfrica, y Argentina. Los estudios fueron suspendidos en octubre por reacciones adversas posibles en un voluntario, pero se reanudaron.
Una de las vacunas chinas
En el caso de Sinopharm, la vacuna de origen chino que se está testeando en la Argentina a través de la Fundación Huésped, no hay un preacuerdo, sino conversaciones que aún no han arribado a una conclusión. La vacuna ya tiene autorización provisoria en China y fue aplicada en más de 300 mil personas, además de en su país de origen, en Emiratos Árabes Unidos, Bahrein, Perú, Marruecos, Pakistán, Serbia y Jordania.
COVAX
Por otro lado, la Argentina pagó a COVAX el anticipo por 9 millones de vacunas. ¿Por qué llevar a cabo tanto una negociación uno a uno, privada, como la participación en la plataforma para países en desarrollo? “Porque nuestra estrategia es tener más dosis cuanto antes y garantizarnos que sean de diferentes candidatas vacunales para cubrir la demanda”, aclara González García.
Y es que además hay otra razón, muy simple: al no saber qué candidata será la que tenga los mejores resultados y sea aprobada, es estratégico poder garantizarse dosis por adelantado de la mayor cantidad de candidatas, en caso de que solo una o un puñado de ellas, llegue a buen puerto y sea o sean aprobadas.

Compras en el mundo
Las compras anticipadas y las negociaciones con los laboratorios que van en punta en el desarrollo de vacunas son una constante, ya desde mediados de año. Algunos ejemplos.
En el mes de julio, los desarrolladores de la candidata vacunal de Pfizer/BioNTech libraron un contrato con el gobierno de los Estados Unidos por 1.900 millones de dólares, que le garantizarían a ese país 100 millones de dosis “en diciembre”, con la opción de otros 500 millones de dosis. También Japón negoció, esta vez por 120 millones de dosis. Y la Unión Europea acordó comprar 200 millones.
En agosto, el gobierno estadounidense aportó a la empresa biotecnológica Moderna 1.500 millones de dólares a cambio de 100 millones de dosis. Y esa biotecnológica (que es la ha dado a conocer el precio más caro hasta ahora para su vacuna, unos 30 dólares la dosis) también concretó acuerdos con Canadá, Japón y Qatar, aún cuando recién el mes pasado terminó de reclutar las 30.000 personas que participan de los ensayos clínicos.
Otro laboratorio que tiene una candidata vacuna en fase 3, Janssen/Johnson & Johnson, recibió mil millones de dólares otra vez de los Estados Unidos por 100 millones de dosis. La Unión Europea llegó a un acuerdo similar el 8 de octubre por 200 millones de dosis. Sin embargo, el 12 de octubre, el laboratorio anunció que puso en pausa sus ensayos clínicos para investigar una reacción adversa en un voluntario. Los testeos se retomaron once días después.
También la vacuna elaborada por Oxford/AstraZeneca ha tenido ventas adelantadas sujetas a evolución de las pruebas y de la aprobación correspondiente y también tuvo pausa en sus testeos debido a reacciones adversas en dos personas. Los ensayos fueron retomados.
En el caso de la Sputnik V, hay excepticismo porque los estudios publicados en la revista médica científica The Lancet en septiembre sólo mencionan un puñado de casos y los pedidos de mayor información realizados por revisores científicos no han sido respondidos con claridad.

En la Argentina las conversaciones siguen (la provincia de Buenos Aires comenzó con ellas también, a mediados de año y con diferentes actores), mientras se analiza qué candidatas se adaptan mejor a las características del país. Por ejemplo, algunas candidatas vacunales (por la tecnología con la que están fabricadas, como en el caso de la elaborada por Pfizer/BioNTech) necesitan contar con cadena de super frío, es decir que exigen ser mantenidas a menos de 80 grados hasta el momento de ser aplicadas a una persona. Un requisito complejo para la Argentina.
Más allá de las consideraciones especiales, ninguna vacuna podrá ser aplicada sin que la evidencia científica la valide. Sin que organismos controlantes la estudien y aprueben.
Pero atentos a la infraestructura que se precisa, la estrategia debe estar lista para salir a vacunar al día siguiente de cualquier aprobación o, al menos, lo más pronto posible. Y en la Argentina, antes de que llegue el próximo invierno con la amenaza de una segunda ola de Covid-19.























Comentarios